Decides aplicar sobre el nuevo lienzo ese pigmento de color rojo que tanto te gusta. Cuando terminas de cubrir su superficie, retiras la pintura con agua. El lienzo recobra la blancura inicial, a excepción de un intenso trazo rojo que resiste tercamente. Repites el mismo proceso con pintura amarilla, verde, morada y azul hasta que el blanco original desaparece. Ante tus ojos, ha emergido una imagen. Los pigmentos se han anclado siguiendo un orden misterioso, como si cada color supiera dónde debía fijarse. Delante de tus narices, y sin que tu lo esperaras, se ha producido la conexión atómica.
En Cuentos de vacaciones, relatos con los que iniciaba El arte de la tinción (I), uno de los personajes de Ramón y Cajal, provisto con sus retinas de aumento, visita el Museo del Prado. El hombre esperaba paz y sosiego en aquel entorno de belleza y armonía, pero su reciente agudeza visual de nuevo le impide disfrutar lo que es creado para el ojo humano corriente. Las sutiles pinceladas de virtuosos artistas se le muestran ahora como burdos brochazos. Las suaves texturas ahora se asemejan a superficies lunares, cuyas grietas e irregularidades le resultan insoportables. No disfruta del horrendo espectáculo en que se ha transformado la pinacoteca. Las obras ya no le ofrecen las sutilezas cromáticas y compositivas que antes estimulaban su intelecto y calmaban su alma. Pobre Juan y su destino.
UN HOMBRE DE SU TIEMPO
De nuevo Ramón y Cajal escribe sobre lo que el sabe que encierra la realidad, no solo habla de los que le descubre su microscopio, sino por lo que le descubren las lecturas de otras áreas de la ciencia. Pero al releer este relato, esta vez con la mirada de una química, algo llamó mi atención: el autor describe con detalle microorganismos, enfermedades y tejidos, pero no profundiza en el mundo molecular y atómico. Y es completamente lógico si se considera el contexto en el que fue escrito. El gran salto de la química aún no se había producido: la estructura del átomo no estaba definida y apenas se empezaba a teorizar sobre la estructura molecular.
Esto me lleva a preguntarme cómo habría sido este cuento si el autor hubiera sabido que los pigmentos se fijan al lienzo mediante enlaces químicos, igual que los tintes a las neuronas de su laboratorio. Qué experiencias habría vivido Juan si su creador hubiera conocido que los electrones son los protagonistas de las uniones entre los átomos. A qué mundos subatómicos nos habría conducido Ramón y Cajal si la mecánica cuántica hubiera estado desarrollada en 1905. Lamentablemente, ese cuento nunca lo leeremos, pero entre las líneas de este post algo sobre la conexión atómica podras descubrir.
LA CONEXIÓN ATÓMICA
El enlace químico es el concepto que describe la unión de los átomos. Estas pequeñas interacciones proporcionan a la materia la solidez percibida en nuestra escala macroscópica. Si poseyéramos la agudeza visual de Juan, podríamos ver cómo se constituye realmente la materia: núcleos atómicos de elementos distintos, mantenidos a cierta distancia, compartiendo zonas periféricas donde los electrones se ubican transitoriamente.
La conexión atómica, fuerte o débil, temporal o permanente, espontánea o forzada, es la base que sostiene nuestra existencia y la del planeta. Llegar a conocer y controlar los enlaces químicos ha sido un gran hito para la humanidad. Hoy en día, industrias de distintos sectores basan sus negocios en sustancias químicas diseñadas a la carta, creadas al unir átomos de forma deliberada. Saber qué átomos se pueden unir, y en qué condiciones, es fruto del conocimiento acumulado por generaciones de químicos y químicas. Es algo que no se puede determinar a simple vista, por lo que se ha requerido mucho trabajo deductivo e ingenio.
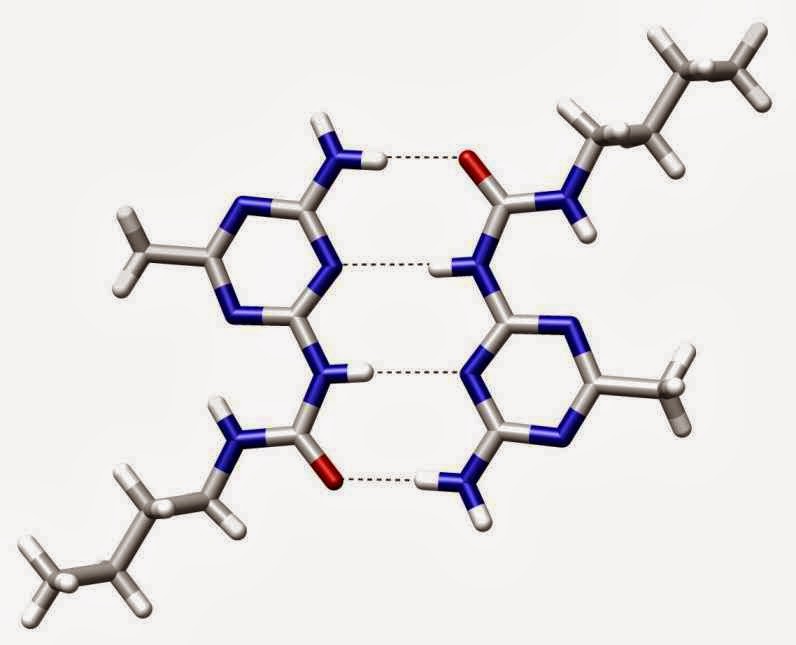
Fuente: Wikipedia
LA CONEXIÓN ATÓMICA DE LOS COLORANTES
Las moléculas, naturales o sintéticas, están formadas por átomos que, según sus características y su organización, crean densidades de carga positivas (d+) y negativas (d-) en la estructura. La presencia de esas densidades de carga es lo que hace que se produzca la interacción con otras moléculas. Estas interacciones son en ocasiones tan fuertes, que se forma una nueva molécula (enlaces covalentes). En otras ocasiones son más débiles, haciendo que queden unidas pero manteniendo su propia identidad (enlaces de hidrógeno o fuerzas de Van der Waals).
Esto último es lo que ocurre en las tinciones químicas de muestras orgánicas (existen otras tinciones). Cuando el colorante tiñe la muestra, es porque uno o varios de sus átomos se han conectado con átomos de alguna biomolécula. Aunque puede darse diferente tipos de enlaces, uno de los más comunes es el enlace de hidrógeno.
# El enlace de hidrógeno: una conexión atómica especial
El enlace de hidrógeno se forma cuando un átomo de hidrógeno (H) unido a un átomo muy electronegativo (X: oxígeno, flúor, nitrógeno) interacciona con otro átomo muy electronegativo ubicado en otra molécula o en otra parte de la misma.
El motivo de esta interacción de se debe a que H y X no comparten por igual los electrones del enlace que los une (H-X): el átomo electronegativo retiene con más fuerza los electrones del enlace. Esta distribución desigual de carga entre ellos, provoca que sientan una atracción hacia otros parejas similares H-X: los hidrógeno (con d+) interaccionan con el X (d-) de la otra pareja, sin comprometer la unión inicial.
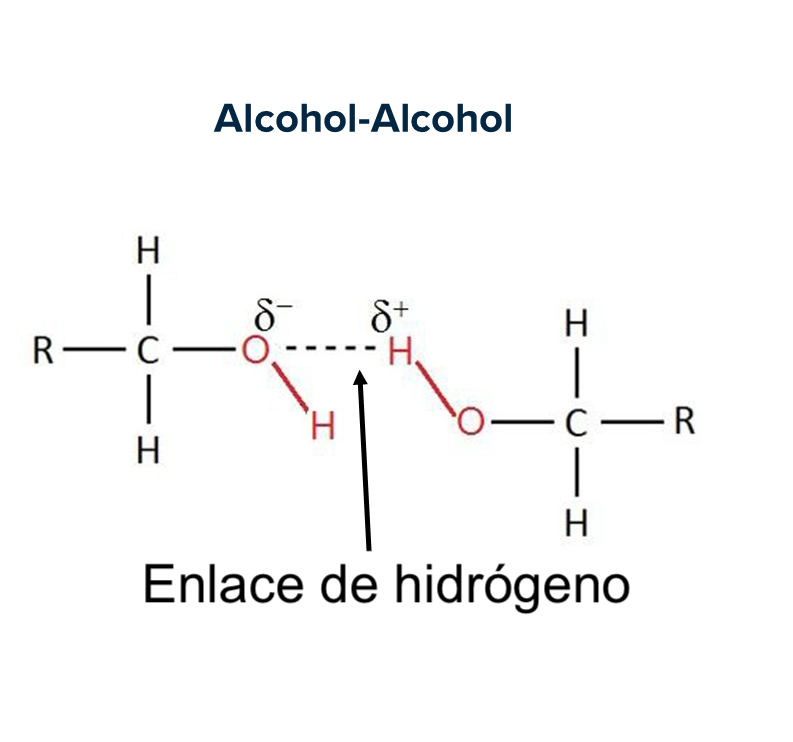
Fuente: www.studysmarter.es
Aunque más débiles que el enlace original (covalente), estas nuevas uniones son lo bastante fuertes como para mantener las moléculas unidas. Al enlace de hidrógeno le debemos, por ejemplo, la presencia de agua líquida en la tierra, la unión de las dos hélices que forman el ADN y la estructura terciaria de las proteínas. Vaya, que no es ninguna tontería.
EL ORO ROJO, EL COLOR DE LOS REYES
Uno de los primeros colorantes usados en la tinción muestras histológicas fue el carmín. Y esto no es de extrañar, ya que era un pigmento muy habitual tanto en los talleres textiles de Holanda y Francia como en las paletas de grandes artistas como Vermeer, Tintoretto o Durero. El principal motivo de su popularidad se debía a que proporcionaba un color rojo de inigualable belleza e intensidad.
# Origen del carmín
Los sumerios y otras antiguas civilizaciones ya usaban el carmín para teñir telas y objetos. Para ello extraían el ácido kermésico de los huevos del insecto Kermes. Se sabe que en Europa también se producía este tipo de carmín desde la Edad del Hierro, introducido supuestamente por los fenicios en torno al s. I a.C.
Las culturas precolombinas Maya, Inca y Azteca, ya desde el s. II a.C., desarrollaron su propia técnica para producir carmín a partir de la cochinilla, parásito del nopal y originario de América Central y México. Tras la extracción del ácido carmínico y posterior tratamiento con alumbre, obtenían el llamado carmín de cochinilla, cuyo color era mucho más intenso y duradero que otros obtenidos de otras especies animales o vegetales. Estas culturas usaban el preciado carmín en los ropajes de los poderosos y en sus fantásticos mapas.

# El rojo mexicano
En el 1523, y debido a la colonización de América, llegaron a Europa noticias sobre el brillante y misterioso carmín de cochinilla mexicano. España monopolizó, tanto la receta como el comercio de este tinte, durante 300 años. Hacia 1820, debido a los problemas en las colonias, y el miedo a perder este rentable negocio, enviaron a Cádiz chumberas cargadas con cochinillas. Unos años después comenzó su cultivo en Canarias. Mientras tanto, otros europeos intentaron, sin mucho éxito, formar parte del negocio. En 1770, el botánico Sir John Hill, tras sus viajes por América, divulgó por Europa lo que descubrió sobre los usos textiles del carmín.
No fue sino hasta un siglo después que comenzó su uso en laboratorios, cuando el médico Joseph von Gerlach, en 1858, estableció un procedimiento estándar para teñir tejidos animales y vegetales con carmín.
# Ácido carmínico
Desde el punto de vista químico, el ácido carmínico, componente principal del carmín de cochinilla, es un C-glucósido derivado de la antraquinona. La antraquinona aislada es incolora e insoluble en agua y alcohol, pero dispone de tres anillos aromáticos fusionados con dos grupos cetónicos centrales. Esta estructura constituye un sistema pi-extendido de electrones que actúan como una verdadera antena de radiación UV. Debido a esto, la naturaleza ha usado la antraquinona como base para la creación de diversos colorantes, como los ácidos carmínico y quérmico.
Fuente: Wikipedia
Hoy en día se sabe que algunos grupos funcionales, llamados cromóforos, desplazan hacia el visible la radiación absorbida por sistemas como la antraquinona. Los fotones del rango visible que no son absorbidos al llegar a nuestra retina son reconocidos como color. En el ácido carmínico el grupo cromóforo es el ácido carboxílico (-COOH), que además mejora su solubilidad en agua y aporta su característico sabor amargo. Otros grupos llamados auxócromos, en este caso el grupo hidroxilo (-OH) modulan el color del colorante y son los puntos de anclaje que permiten la fijación a la sustancia teñida.
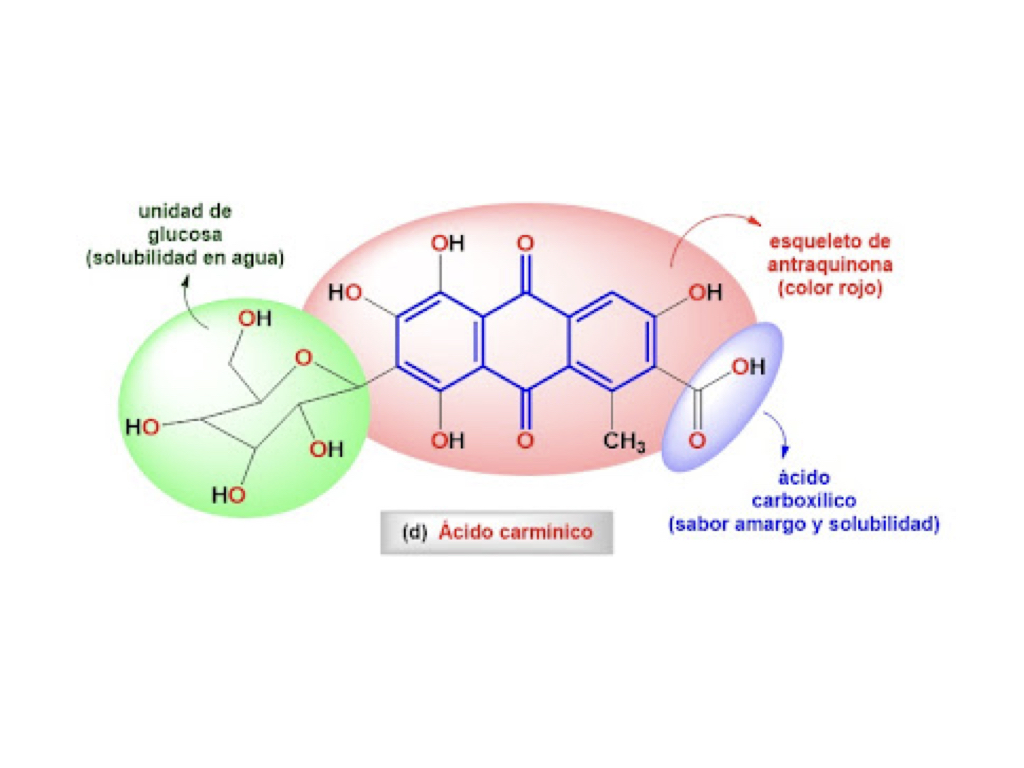
Fuente: UBUScientia
# La composición química de la laca de carmín
Hoy en día, el carmín utilizado en las tinciones es el carmín de best o laca de carmín, que contiene dos ácidos carmínicos unidos por un catión de aluminio. Esta laca es soluble en agua caliente alcalina. Este último actúa como mordiente, facilitando la adhesión del colorante al sustrato.
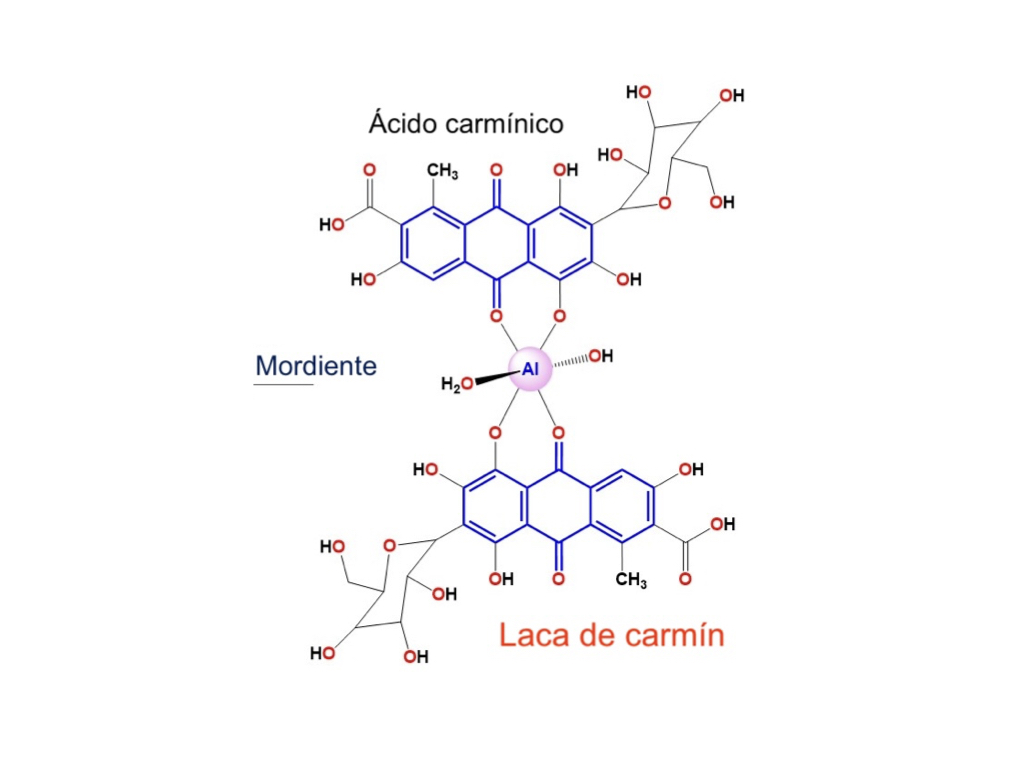
# Conexión atómica: el match entre colorante y biomolécula
El carmín de best tiene afinidad química con el glucógeno. El glucógeno es una biomolécula formada por cadenas ramificadas de glucosa, la molécula que proporciona energía celular. Así, el glucógeno es uno de nuestros almacenes energéticos que se encuentra principalmente en el hígado, los músculos estriados y células gliales del cerebro.
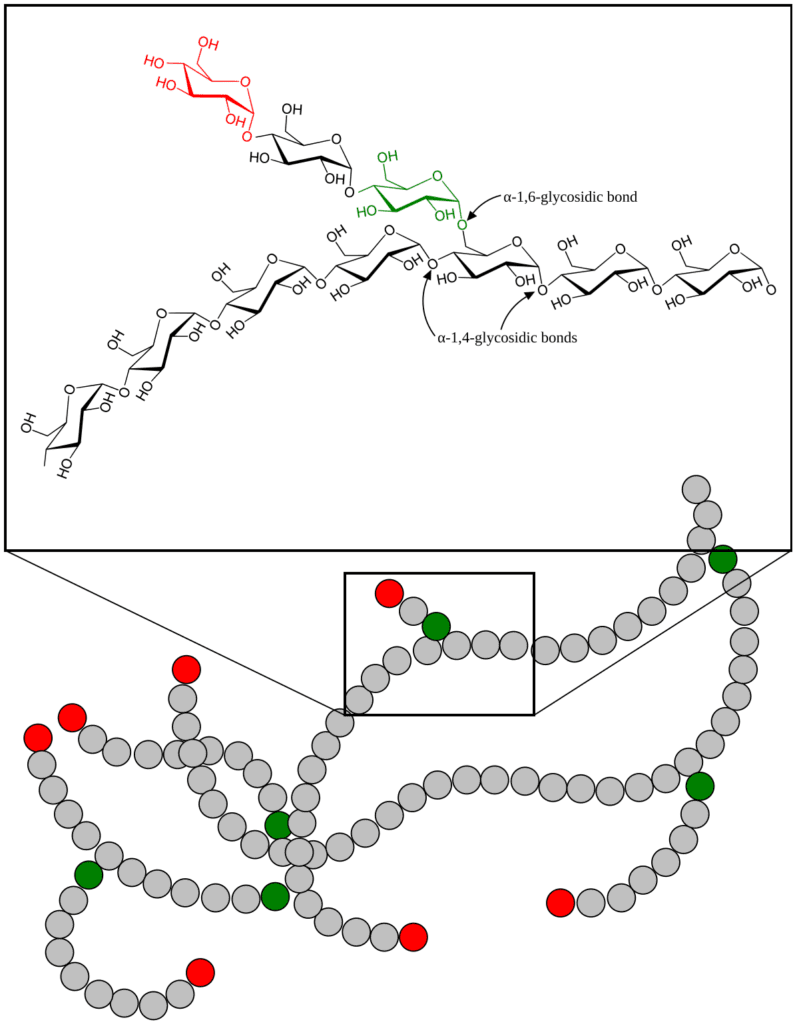
Fuente: Wikipedia
Cuando el ácido carmínico entra en contacto con una cadena de glucógeno, sus grupos carboxilo e hidroxilo interactúan con los grupos hidroxilo del glucógeno, formando enlaces de hidrógeno que mantienen unidas ambas estructuras. He aquí la conexión atómica. En la laca de carmín, el aluminio actúa como mordiente, un intermediario que facilita la unión, haciéndola más estable y más intensa.
CARTOGRAFIANDO NUESTRO INTERIOR
Desde el primer uso del carmín en histología para teñir células vegetales, la búsqueda de nuevos colorantes para teñir células y tejidos ha sido constante. Hoy, la variedad de colorantes es tan amplia y su especificidad tan precisa que es posible cartografiar tejidos y microorganismos detalladamente.
El nivel de perfección y control de las técnicas es tan alto que las imágenes obtenidas con la tinción son verdaderas obras de arte. Si te interesa verlas, no te pierdas el siguiente post: El arte de la tinción (III).
MATERIAL DE CONSULTA
Vídeos y enlaces recomendados:
- UBUScientia. Blog de la Universidad de Burgos.
- Web World History Encyclopedia (en español)
- Usos de colorantes en histología vegetal y animal. Blog de la Universidad de Vigo
Libros y artículos
- Introducción a la Química de los Colorantes. Deanna Marcano.
- Cuentos de vacaciones. Santiago Ramon y Cajal.
Imagen: Fuente: imagen creada con inteligencia artificial. Gemini.


Deja una respuesta