Mira a tu alrededor y fíjate en los objetos que te rodean. Quizá te llama la atención la agenda roja, la taza de café azul celeste o las flores fucsia de tu planta favorita. Bajo la aparente quietud de todos esos pigmentos, a nivel cuántico están ocurriendo fenómenos fascinantes. Y es en los sutiles saltos energéticos de los electrones de los grupos azo, anillos aromáticos y carbonilos que forman parte de su estructura, donde se esconde el origen de ese fenómeno sensorial que define nuestra percepción del mundo: el color.
No hace más de dos siglos que químicos y químicas comenzaron a comprender la naturaleza de los colores. Una de las primeras personas en relacionar la estructura molecular y el color fue Otto Nikolaus Witt, quien en 1876 escribió que el color tendía a aparecer en moléculas orgánicas no saturadas. Esta descripción en realidad hacía referencia a grupos funcionales que contenían en su estructura enlaces dobles y triples, y que actualmente reciben el nombre de cromóforos.
Previamente a esta conceptualización química del color, ya se habían hecho contribuciones importantes a nivel experimental. Una de ellas fue la realizada por William Henry Perkin, quien, en 1856, sintetizó el primer colorante artificial, la mauveína, dando inicio así a la Química de los Colores.
La lista de aplicaciones de colorantes es extensa, diversa y, en algunos casos, controvertida, como es el caso de su uso en alimentos. Pero el objetivo de este blog no es hablar del lado oscuro de las sustancias químicas, sino sacarlas al escenario y mostrar quiénes son. En esta publicación el foco de luz estará dirigido a una familia química muy especial.
Hoy es el turno de los colorantes azo.

EL PAISAJE MOLECULAR
Dos de los principales protagonistas del color son los electrones y los fotones. Cuando un pigmento es iluminado, algunos de sus electrones se movilizan por la acción de los fotones. Pero estos no actúan solos. El paisaje donde se encuentran desempeña también un papel crucial en el desarrollo del color. En el caso de los compuestos orgánicos, este “paisaje” está definido por la estructura molecular de la sustancia.
# El cromóforo, el Don Quijote del colorante
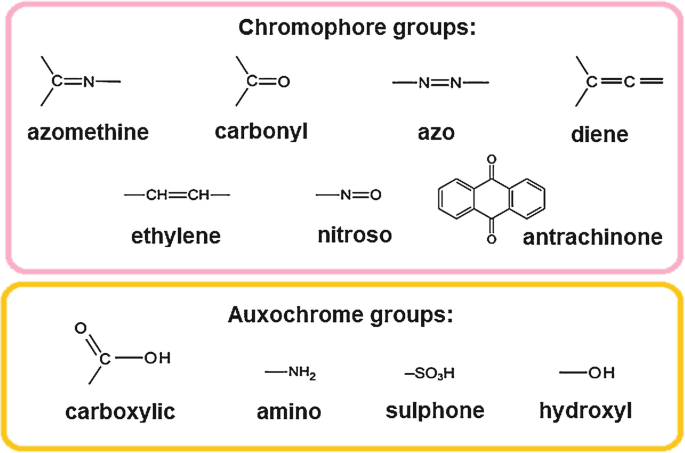
Tras estudiar con detalle las estructuras de los colorantes orgánicos se ha llegado a la conclusión de que las propiedades cromáticas se deben a unos grupitos de átomos denominados grupos cromóforos. El tipo y número de grupos cromóforos determina tanto la tonalidad cromática como su intensidad.
Los cromóforos más habituales son el grupo carbonilo (-C=O), el grupo nitro (-NO2), los doble etilenos (-C=C-), el grupo nitroso (-N=O) y el grupo azo (-N=N-)
# El auxócromo, el Sancho Panza del cromóforo
El comportamiento de los grupos cromóforos está condicionado por el resto del paisaje molecular, en concreto por los grupos auxócromos, quienes influyen en la interacción luz-cromóforo.
Los grupos auxócromos más habituales son el grupo hidroxilo (-OH), el grupo amino (-NH2) y el grupo carbonilo (-COOH). La naturaleza ácida y básica de estos grupos hace que el pH del medio también participe en el desarrollo del color, al promover la formación de cargas negativas y positivas en los grupos ácidos, como el COOOH, o básicos como el NH2 respectivamente.
EL CROMÓFORO EN ACCIÓN
Cuando la luz solar ilumina un cromóforo, algunos de los fotones lumínicos quedan retenidos en él. Son los denominados fotones absorbidos. Solo quedan atrapados aquellos fotones que tienen cierta energía, el resto son reflejados.
Los fotones reflejados son los que detectará mi retina y los que proporcionarán la información que mi cerebro traducirá en color y otras propiedades ópticas. De este modo, si el cromóforo absorbe fotones de energía del rango del espectro visible asociado al color verde, el color que yo percibiré lo conformará el conjunto de fotones no absorbidos reflejados, y que en este caso mi cerebro percibirá como rojo, su complementario.
La presencia o ausencia de ciertos grupos auxócromos puede favorecer o dificultar la absorción de fotones. Por ejemplo, un auxócromo puede hacer que un grupo cromofóro, que suele absorber fotones verdes, absorba fotones azules. En este caso el color que percibiré por mi ya no será rojo, sino más anaranjado. También hay grupos cromóforos que no son visibles para el ojo humano, porque absorben fotones del ultravioleta, pero que se vuelven visibles bajo la influencia de ciertos auxócromos.
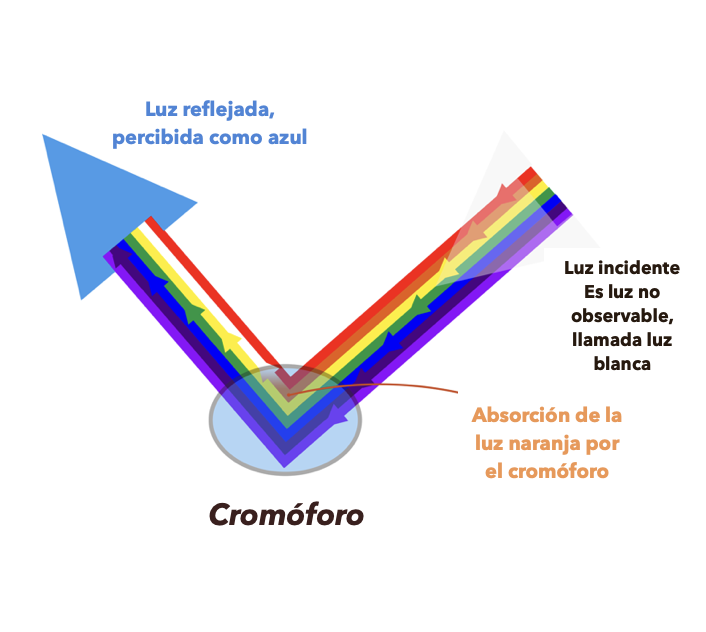
de luces será percibido como azul claro (complementario).
LA ARQUITECTA DE LA QUÍMICA: la síntesis orgánica
El descubrimiento de todas estas estructuras y el análisis de su comportamiento frente a la luz constituye el núcleo duro de la industria de los colorantes. Pero una vez conocidas sus propiedades, para crear un colorante o pigmento funcional, es necesario ensamblarlas estas estructuras con otras que aporten propiedades diferentes: solubilidad en un medio; estabilidad frente a la oxidación; estabilidad térmica y actividad biocida entre otras.
Es en este punto donde entra en juego la síntesis química orgánica, que dispone de las herramientas para diseñar estructuras moleculares o poliméricas y sintetizarlas mediante el ensamblado de fragmentos o precursores.
Si has llegado hasta aquí, es posible que te estés preguntando: ¿qué tienen de especial los grupos cromóforos para atrapar los fotones de luz?
La respuesta es sencilla: alta densidad electrónica pero deslocalizada.
EL GRUPO AZO, EL NIÑO DE MIS OJOS
Uno de mis grupos cromóforos favoritos es el grupo azo. Me fascinan sus colores y su estructura química, que se caracteriza por un núcleo formado por una pareja de átomos de nitrógeno. Me fascina también su singular ausencia en la Tierra, donde el nitrógeno suele estar presente en otras formas químicas más estables. Sin embargo, esta aparente desventaja energética no ha impedido que los laboratorios hayan conseguido sintetizar azoderivados de gran estabilidad.
El grupo azo está constituido por dos átomos de nitrógeno unidos por un enlace doble (-C-N=N-C-). Al igual que el resto de enlaces dobles, este se compone de dos pares de electrones: uno fijo entre los nitrógenos y el otro con cierta movilidad. Además, cada átomo de nitrógeno tiene un par de electrones sin enlazar. Como resultado, el grupo azo cuenta con un total de seis electrones deslocalizados, lo cual significa que estos electrones no están fijos en una ubicación específica dentro de la molécula, sino que tienen cierta libertad para moverse a través de la estructura.
Para moverse, estos electrones requieren de un impulso externo, es decir, de energía. Una forma de obtenerla es mediante los fotones de luz. Solo se necesita una condición: que los fotones cuenten con la energía exacta -ni más, ni menos- que permita que los electrones salten a los llamados estados excitados. Cuantos más electrones estén disponibles para este salto, mayores serán las probabilidades de que ser produzca la absorción de fotones y, en consecuencia el desarrollo de color.
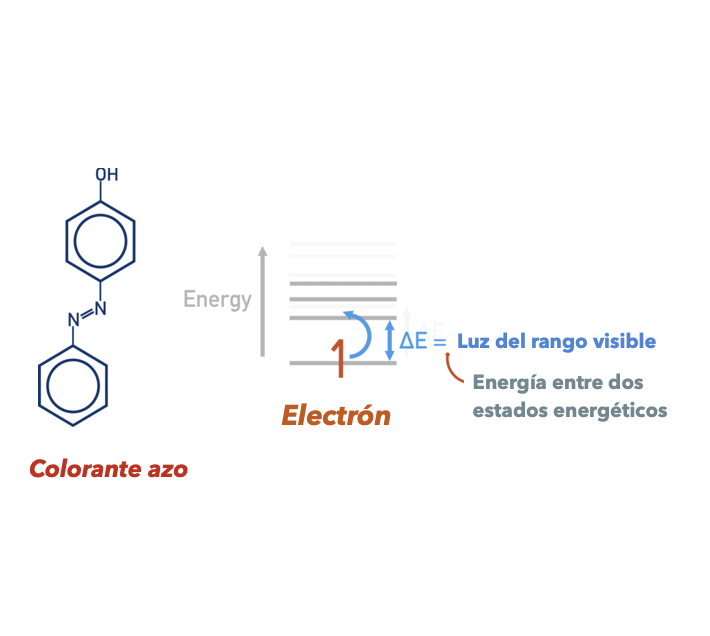
Fuente: www.chemistrystudent.com
Pero no todas las moléculas con grupo azo presentan coloración. Algunas son incoloras. Entonces, ¿cuáles son los azoderivados ideales para ser colorantes?
UN AZO DERIVADO CON ARILOS, POR FAVOR
Se estima que existen alrededor de 3000 colorantes azo. De ellos, aproximadamente el 60-70% son conocidos como aril derivados, lo que significa que uno o ambos lados del grupo azo están unidos a anillos aromáticos. Estos anillos facilitan la deslocalización de los seis electrones móviles del grupo azo y, además, reducen la energía de los estados excitados, lo que permite que se necesiten fotones de menor energía para excitar los electrones.
De este modo, los anillos aromáticos y los grupos funcionales que los acompañan actúan como un “refugio” adicional para los electrones, favoreciendo su movimiento a través de la molécula y su acceso a niveles de energía superiores.
LOS COLORES DE LOS AZO
Los colorantes azo son conocidos por sus brillantes tonos amarillos, naranjas y rojos, como la tartracina, el naranja de metilo o el rojo Congo respectivamente. También pueden presentar tonos azules, como es el caso del trisazo, o verdes, como el verde de metilo.
La gran ventaja de las metodologías desarrolladas por la química orgánica es permiten el diseño de moléculas “a la carta”con casi cualquier estructura que podamos imaginar. Esto significa, que pueden crearse moléculas con grupos azo que dispogan de otros elementos capaces de modular los colores antes citados.
Por ejemplo, en la imagen siguiente una molécula presenta dos grupo azo, uno de ello absorbe UV y el otro fotones de la región del verde. Esta característica puede ser de gran utilidad en la fabricación de sensores de luz. Este caso ejemplariza cómo un mismo grupo cromóforo en distintos paisajes, tendrá también distinto comportamiento frente a la luz.
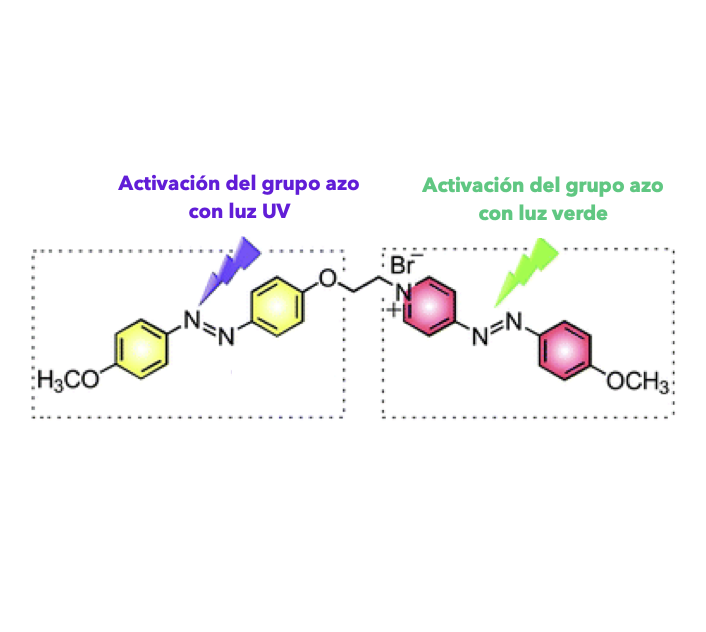
Fuente: Chemical Communications, 78, 2014.
Aún queda una pregunta por responder. Si la naturaleza no ha sido la proveedora de los grupos azo, ¿cómo se han obtenido?
CREANDO EL GRUPO AZO
El grupo azo vio la luz en un laboratorio, al menos de forma estable. Existen varios procesos de obtención de grupos azo, pero el más famosos es el acoplamiento azoico. El proceso estándar consiste en dos pasos principales, aunque ya hay disponibles variantes del proceso.
# Ensamblado de dos átomos de nitrógeno.
Como resultado de esta unión se forma la denominada sal de diazonio. El proceso requiere varias etapas:
- Formación del reactivo ácido nitroso (HNO2), mezclando nitrito de sodio (NaNO2) y ácido clorhídrico (HCl).
- Formación de una nitrosamina por reacción del ácido nitroso y una amina aromática (anilina).
- Evolución de la nitrosamina a la sal de arildiazonio.
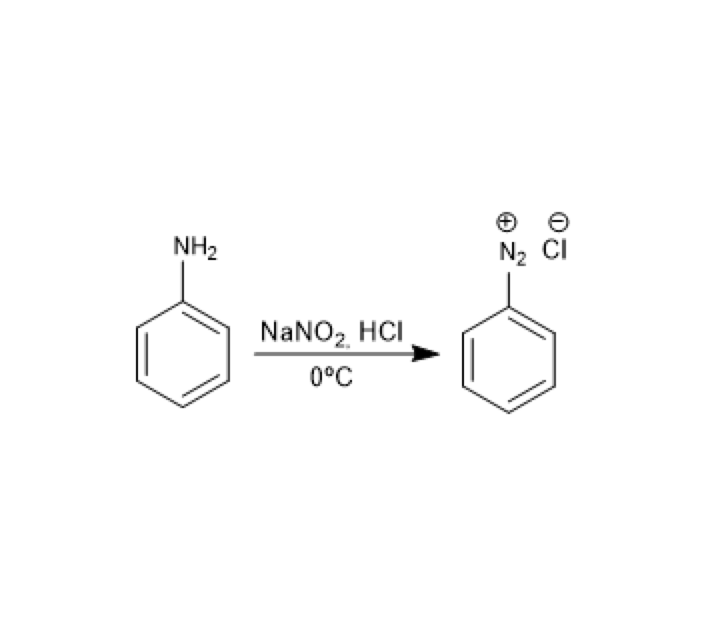
Fuente: www.quimicaorganica.net
# Acoplamiento azoico.
Esta etapa consiste en ensamblado de un anillo aromático a uno de los átomos de nitrógeno de la sal de diazonio. Las sales de diazonio son compuestos electrófilos, lo que significa que se sienten atraídos por cargas negativas y pares de electrones no enlazados. Así, uno de los átomos de nitrógeno de la sal de diazonio se une a un anillo de fenol (que actúa como nucleófilo), debido a que este último es rico en electrones.
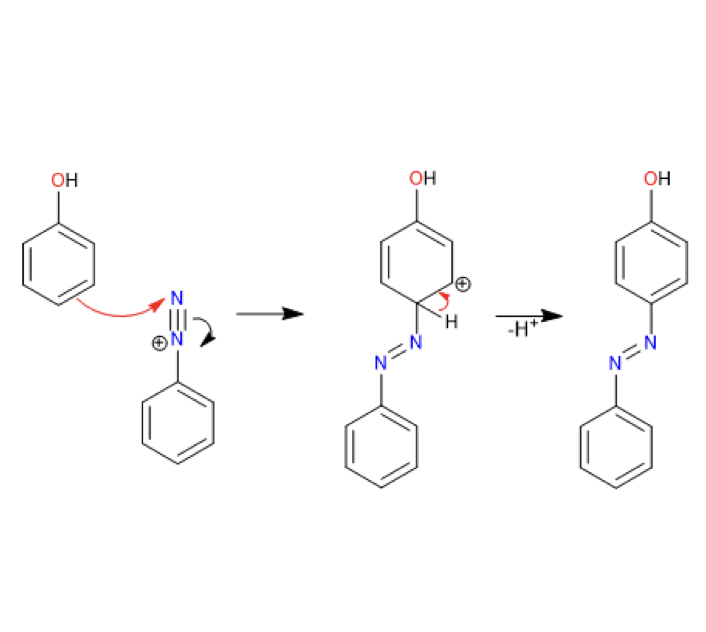
Fuente: www.quimicaorganica.net.
LA MAGIA DEL COLOR
Dar color a los objetos, ya sean cuerpos, rocas, pieles o lienzos, es una habilidad que el ser humano ha sabido desarrollar a lo largo de los milenios. Y fue la naturaleza quien durante mucho de este tiempo suministró la materia prima de estos colores. Hasta que la mano humana decidió intervenir y crearlos a su gusto.
Los azoderivados son un claro ejemplo de nuestra intervención. Lo que comenzó como un experimento ha terminado en un extenso catálogo de colores con una amplia gama de aplicaciones.
Ahora ya no es un secreto que el color de estas sustancias delata lo que está ocurriendo internamente. A partir de hoy, cuando veas un rosa, un verde o un ocre sabrás que el viaje cuántico de los electrones ya ha comenzado.
MATERIAL DE CONSULTA
Vídeos y enlaces recomendados
- Blog de Química Orgánica de la Universidad de Oviedo.
- Estructuras moleculares de colorantes azoicos.
Libros y artículo
- Introducción a la Química de los Colorantes. Deanna Marcano.
- Conceptos básicos de los colorantes azoicos basados en el 2-aminotiazol. Sejal Patel.
- New Azo Disperse Dyes Derived from 3-(Hydroxyphenyl)-2-pyrazolin-5-one Tapa blanda, 2013. Moaz M. Abdou.
Imagen: creada con inteligencia artificial (Gemini).
Gracias por leer hasta aquí.
¡Espero que hayas encontrado útil y entretenido este post!
Para seguir leyendo, te recomiendo visitar la página de entradas del blog.


Deja una respuesta